二零二四年一月 第三期
有得食又有得玩的家中科學實驗
在初中科學科中,我們學到水會在不同物態間轉換。今天筆者將教大家在家中進行簡單科學實驗,探究水和牛奶在不同物態之間的變化。完成實驗後,我們會得到凝固的抹茶牛奶,灑上開心果碎後就成為抹茶開心果牛奶沙冰,既可以做實驗也不會浪費食物。文末附上實驗材料和工具,歡迎讀者在家中一同安全地進行科學實驗。

實驗步驟:
- 將400毫升牛奶與抹茶粉及煉奶混合,然後平均倒入兩個密實袋,封口備用。
- 將300克冰塊倒入大碗甲(實驗組),另外300克冰塊則倒入大碗乙(對照組)。
- 量度及記錄兩個大碗內冰塊的溫度。
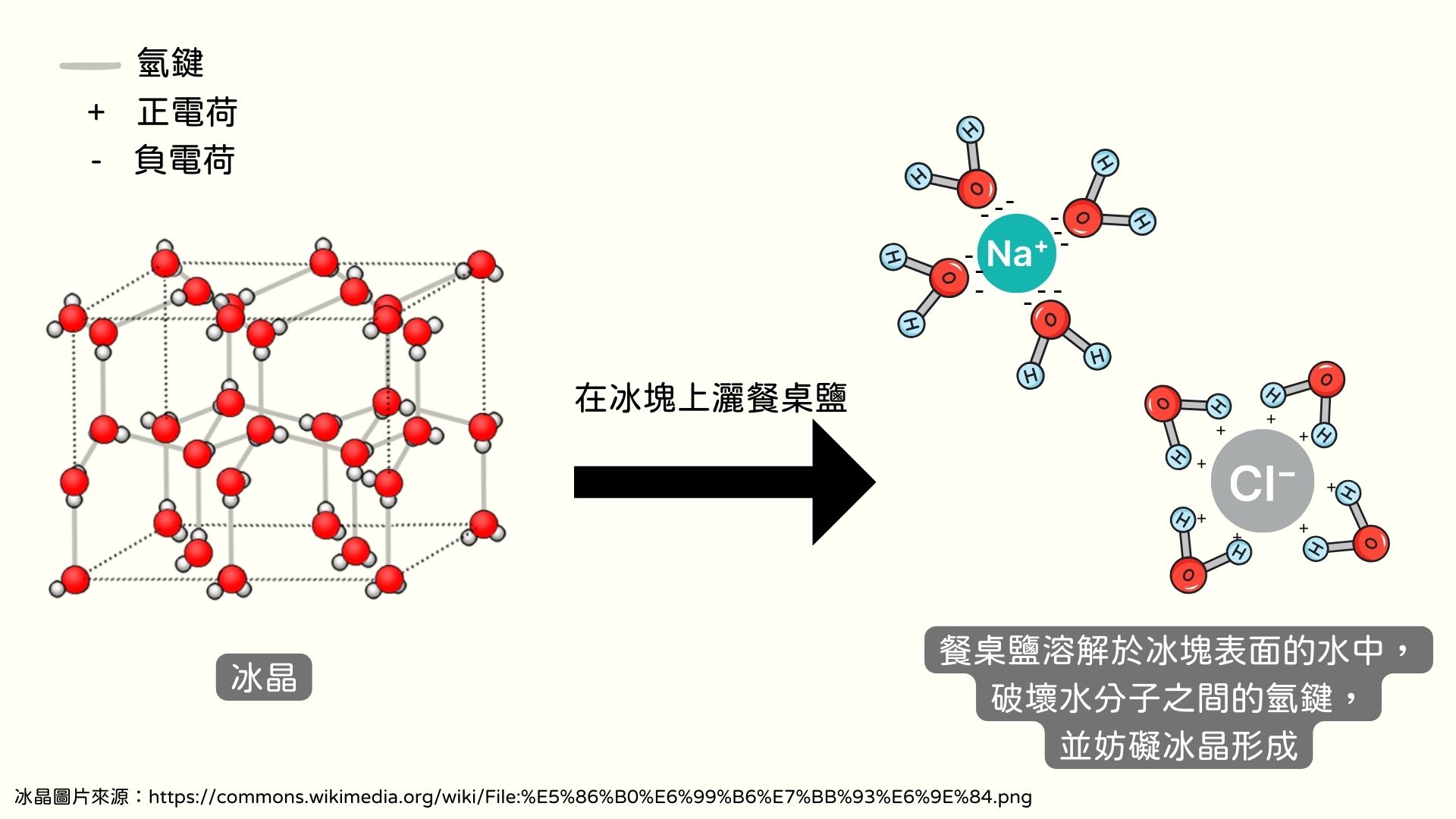
- 在大碗甲內的冰塊表面灑上餐桌鹽,並用筷子攪拌均勻。
- 將兩個裝有抹茶牛奶的密實袋分別放入大碗甲和大碗乙,並將冰塊蓋上密實袋。
- 每隔2分鐘量度及記錄大碗內冰水的溫度。
- 10分鐘後,取出密實袋,觀察牛奶的形態。
- 完成實驗後,在凝固的牛奶沙冰上灑上開心果碎後即可食用。
在這次實驗中,我們能觀察到三個現象:一,浸泡在大碗甲中的牛奶會凝固成固體,而浸泡在大碗乙的牛奶則不會凝固;二,在實驗開始時,兩個大碗內冰塊的溫度均為0°C,但隨後大碗甲內的水溶液(鹽水)的溫度逐漸降低至零下14°C,而大碗乙則依然為0°C;三,大碗甲的表面有霜形成,而大碗乙的表面則只有液態水珠凝結。



為何鹽水能降至零下14°C也不會結冰?接下來,我們將會逐項現象解釋。首先,當水凝固成冰時,每一個水分子都以四個氫鍵連接四個周圍的水分子,形成冰晶,此時水的凝固點為0°C。當我們加入餐桌鹽(氯化鈉)時,鹽溶解於冰塊表面的水中,帶正電的鈉離子與帶負電的氯離子吸引水分子,破壞水分子之間的氫鍵。由於鈉離子和氯離子妨礙冰晶的形成,鹽水的凝固點下降,這能解釋為何大碗甲內的鹽水溫度能低於水本來的凝固點,即0°C。由於大碗甲內鹽水的溫度達-14°C,牛奶的熱能被鹽水吸收,溫度下降至低於凝固點,因而凝固成固體。
至於為何大碗甲的表面有霜形成,原因是大碗甲的表面溫度降至水的凝固點以下,空氣中的水汽聚集在大碗甲表面,並不經過液態直接凝結成冰晶,這個過程稱為凝華。相反,由於大碗乙表面溫度高於水的凝固點,空氣中的水汽凝結成液態水珠,這個過程稱為凝結。
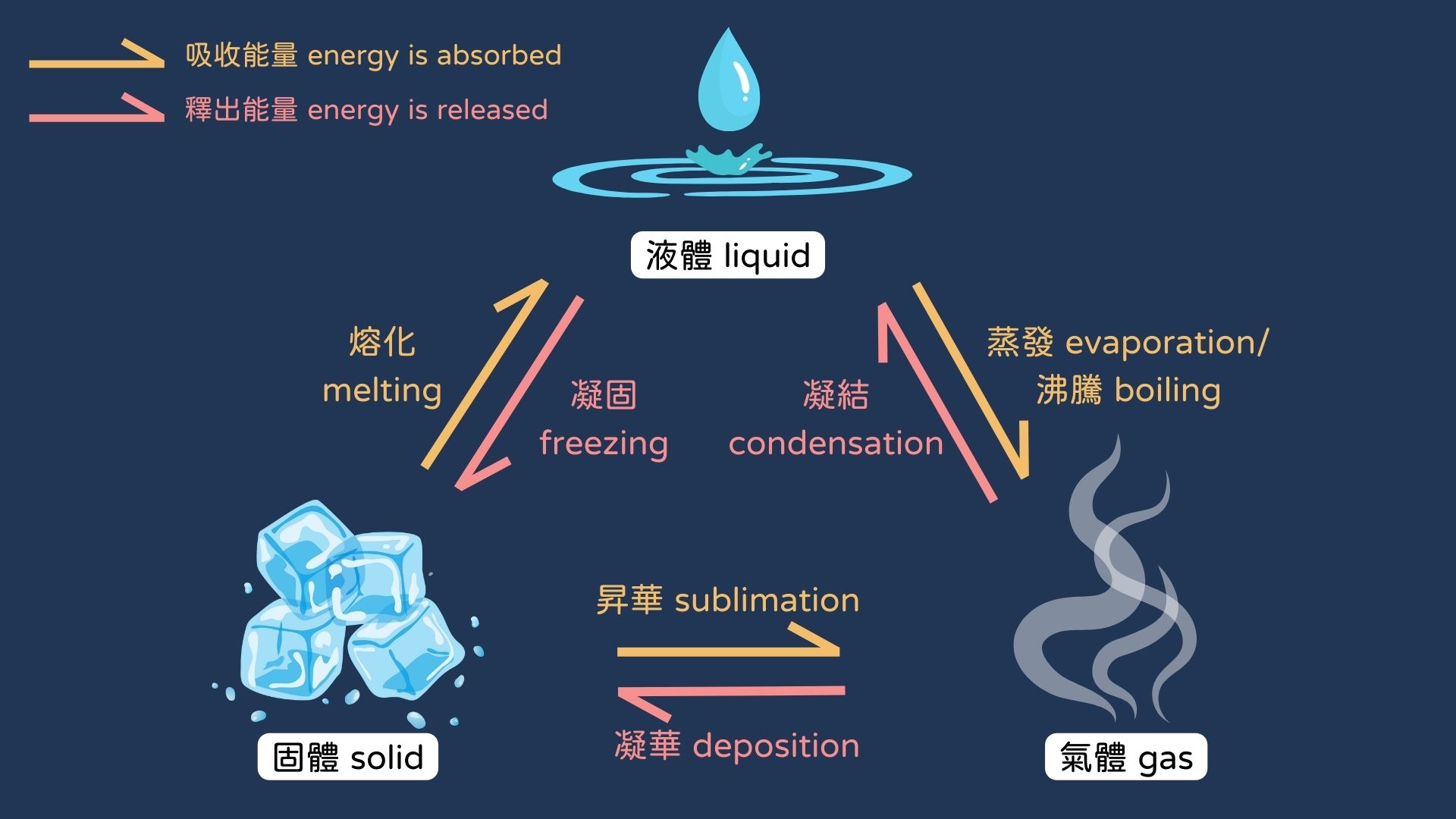
考考大家,如果將更多的餐桌鹽加入相同數量的冰塊中,溫度會有甚麼變化?
實驗材料和工具:
冰塊 600克(實驗組300克+對照組300克)
餐桌鹽 100克
牛奶 400毫升(實驗組200毫升+對照組200毫升)
開心果碎 適量
抹茶粉 適量
煉奶 適量
大碗2個
小型密實袋2個
溫度計2枝
筷子1對
注意事項:
冰塊與鹽混合後溫度會降至攝氏度零下,請小心慎防凍傷。
參考資料
唐宇煇(2010)。香港的結霜天氣。檢自: https://www.hko.gov.hk/tc/education/weather/weather-phenomena/00037-frost-in-hong-kong.html
國立科學工藝博物館科學學習中心(2014)。化學應用:國小-5分冰淇淋。檢自:https://slc.nstm.gov.tw/Teaching/Details.aspx?Parser=99,4,27,,,,228
生物科
詹愷盈老師











